2025知到答案 化学基础与分析技术 最新智慧树满分章节测试答案
绪论 单元测试
1、判断题:
食品加工过程中加入的成分为天然成分。( )
选项:
A:错
B:对
答案: 【错】
2、判断题:
食品中加入适量的防腐剂可延长保质期。( )
选项:
A:对
B:错
答案: 【对】
3、判断题:
肉类、鱼类主要成分是碳水化合物。( )
选项:
A:对
B:错
答案: 【错】
4、判断题:
人一般不吃不喝能坚持十天。( )
选项:
A:对
B:错
答案: 【错】
5、判断题:
今后不能考化学检验员证书。( )
选项:
A:错
B:对
答案: 【错】
6、判断题:
食品中固有的成分为天然成分。( )
选项:
A:错
B:对
答案: 【对】
7、判断题:
食品是人类生存的必需物质。( )
选项:
A:错
B:对
答案: 【对】
8、单选题:
化学基础与分析技术是药学或食品。( )
选项:
A:专业扩展课
B:专业课
C:其余选项都不是
D:专业基础课
答案: 【专业基础课】
9、单选题:
实训操作课需要( )实验现象和数据。( )
选项:
A:准确
B:真实
C:其余选项都是
D:及时记录
答案: 【其余选项都是】
10、多选题:
化学是研究物质的( )及其变化规律的基础学科。( )
选项:
A:性质
B:结构
C:应用
D:组成
答案: 【性质;
结构;
应用;
组成】
第一章 单元测试
1、单选题:
1500ml的生理盐水中含Na+( )。
选项:
A:0.59g
B:13.5g
C:9g
D:5.31g
答案: 【5.31g】
2、判断题:
NaCl固体溶解在水溶液中,NaCl是溶质,水是溶剂。( )
选项:
A:对
B:错
答案: 【对】
3、判断题:
物质的量浓度(cB)是单位体积溶液中所含溶质的物质的量与溶液的体积之比。( )
选项:
A:对
B:错
答案: 【对】
4、单选题:
室温下葡萄糖、氯化钠、氯化钙这三种溶液的浓度均为0.1mol/L,渗透压按由低到高顺序是( )。
选项:
A:氯化钙、氯化钠、葡萄糖
B:氯化钠、氯化钙、葡萄糖
C:葡萄糖、氯化钠、氯化钙
D:葡萄糖、氯化钙、氯化钠
答案: 【葡萄糖、氯化钠、氯化钙】
5、单选题:
表面活性剂在结构上具有的特征是( )。
选项:
A:既有亲水性基团,又有亲油性基团
B:只有亲油性基团
C:只有亲水性基团
D:一定有亲水性基团,但不一定有亲油性基团
答案: 【既有亲水性基团,又有亲油性基团】
6、单选题:
硫酸瓶上的标记是80%H2SO4,相对分子质量M=98.0,密度ρ=1.73g·mL-1,下列数值中接近该酸的物质的量浓度的是( )mol·L-1。
选项:
A:16.6
B:10.2
C:9.8
D:14.1
答案: 【14.1】
7、判断题:
物质的量浓度(cB) 常用的单位为mol/L或mmol/L、或mol·L-1 ,mmol·L-1。( )
选项:
A:对
B:错
答案: 【对】
8、判断题:
乳化剂所起的作用称为乳化作用。( )
选项:
A:对
B:错
答案: 【对】
9、多选题:
下列属于粗分散体系的是( )
选项:
A:豆浆
B:牛乳
C:炉甘石洗剂
D:海水
答案: 【牛乳;
炉甘石洗剂】
10、多选题:
渗透产生的条件( )
选项:
A:膜的两侧存在浓度差
B:温度一定
C:半透膜
D:光照
答案: 【膜的两侧存在浓度差;
半透膜】
第二章 单元测试
1、单选题:
在一定条件下,对于密闭容器中进行的可逆反应:N2(g)+3H2(g) 2NH3(g),下列说法中,表明这一反应已经达到化学平衡状态的是( )
2NH3(g),下列说法中,表明这一反应已经达到化学平衡状态的是( )
选项:
A:N2、H2、NH3在密闭容器中共存
B:N2、H2、NH3的浓度相等
C:N2、H2、NH3的浓度不再变化
D:反应停止,正、逆反应速率都等于零
答案: 【N2、H2、NH3的浓度不再变化】
2、单选题:
5.6 g铁粉投入到盛有100 mL 2mol/L稀硫酸的烧杯中,2 min时铁粉刚好溶解(溶解前后溶液体积变化忽略不计),下列表示这个反应的速率正确的是( )
选项:
A:v(H2SO4)=1 mol/(L·min)
B:v(H2SO4)=0.5 mol/(L·min)
C:v(FeSO4)=1 mol/(L·min)
D:v(Fe)=0.5 mol/(L·min)
答案: 【v(H2SO4)=0.5 mol/(L·min)】
3、单选题:
在恒温、恒容的密闭容器中进行反应A(g) B(g)+C(g),若反应物的浓度由2mol·L﹣1降到0.8mol·L﹣1需要20s,那么反应物浓度再由0.8mol·L﹣1降到0.2mol·L﹣1所需要的时间为( )
B(g)+C(g),若反应物的浓度由2mol·L﹣1降到0.8mol·L﹣1需要20s,那么反应物浓度再由0.8mol·L﹣1降到0.2mol·L﹣1所需要的时间为( )
选项:
A:无法判断
B:10s
C:小于10s
D:大于10s
答案: 【大于10s】
4、单选题:
已知下列反应的平衡常数:2Cu (s)+l/2O2 (g) Cu2O (s)为K1,Cu2O (s) + l/2O2 (g)
Cu2O (s)为K1,Cu2O (s) + l/2O2 (g)  2CuO (s)为K2。则反应 2Cu(s)+02(g)
2CuO (s)为K2。则反应 2Cu(s)+02(g)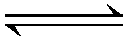 2CuO (s)的K等于:( )。
2CuO (s)的K等于:( )。
选项:
A:K,xK2
B:Kt-K2
C:Kt/K2
D:K1+K2
答案: 【K,xK2】
5、单选题:
反应4NH3+5O2 4NO+6H2O,在5L的密闭容器中进行30秒后,NO的物质的量增加了0.3mol,则此反应的平均速率v(x)为( )。
4NO+6H2O,在5L的密闭容器中进行30秒后,NO的物质的量增加了0.3mol,则此反应的平均速率v(x)为( )。
选项:
A:v (NH3 )=0. 002mol/ (L•秒)
B:v (O2) =0.01mol/ (L•秒)
C:v (H2O) = 0. 003mol/ (L•秒)
D:v (NO) = 0. 008mol/ (L•秒)
答案: 【v (O2) =0.01mol/ (L•秒)】
6、单选题:
设反应C+CO2 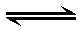 2CO(正反应吸热)反应速率为v1,N2+3H2
2CO(正反应吸热)反应速率为v1,N2+3H2 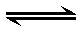 2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为( )
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为( )
选项:
A:v1减小,v2增大
B:v1增大,v2减小
C:同时减小
D:同时增大
答案: 【同时增大】
7、单选题:
在容积固定的密闭容器中充入一定量的X、Y两种气体,一定条件下发生可逆反应3X(g)+Y(g)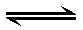 2Z(g),并达到平衡。已知正反应是放热反应,测得X的转化率为37. 5%,Y的转化率为25%,下列有关叙述正确的是( )
2Z(g),并达到平衡。已知正反应是放热反应,测得X的转化率为37. 5%,Y的转化率为25%,下列有关叙述正确的是( )
选项:
A:升高温度,正反应速率减小,平衡向逆反应方向移动
B:若向容器中充入氦气,压强增大,Y的转化率提高
C:若X的反应速率为0.2 mol·L-1·s-1,则Z的反应速率为0.3 mol·L-1·s-1
D:开始充入容器中的X、Y物质的量之比为2∶1
答案: 【开始充入容器中的X、Y物质的量之比为2∶1】
8、多选题:
以下属于有效碰撞理论观点的是( )
选项:
A:分子必须通过碰撞才能发生反应。
B:发生化学反应时,反应物分子间首先形成活化配合物,然后转化为产物。
C:碰撞频率越高,化学反应速率越快。
D:反应气体分子可看做简单的刚性小球,无内部结构。
答案: 【分子必须通过碰撞才能发生反应。;
碰撞频率越高,化学反应速率越快。;
反应气体分子可看做简单的刚性小球,无内部结构。】
9、单选题:
在温度不变的条件下,密闭容器中发生如下反应:2SO2+O2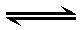 2SO3,下列叙述能够说明反应已经达到平衡状态的是( )
2SO3,下列叙述能够说明反应已经达到平衡状态的是( )
选项:
A:反应容器中压强不随时间变化
B:容器中SO2、O2、SO3的物质的量之比为2∶1∶2
C:容器中SO2、O2、SO3共存
D:SO2与SO3的浓度相等
答案: 【反应容器中压强不随时间变化】
10、单选题:
一定温度下,浓度均为1mol·L-1的A2和B2两种气体,在密闭容器内反应生成气体C,反应达平衡后,测得:c(A2)=0.58 mol·L-1,c(B2)=0.16 mol·L-1,c(C)=0.84 mol·L-1,则该反应的正确表达式为( )
选项:
A:A2+2B2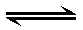 2AB2
2AB2
B:2A2+B2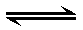 2A2B
2A2B
C:A2+B2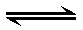 2AB
2AB
D:A2+B2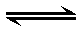 A2B2
A2B2
答案: 【A2+2B2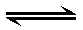 2AB2】
2AB2】
